
Estrutura do óxido de cério (IV), propriedades, usos

O óxido de cério (IV) O óxido cerico é um sólido inorgânico branco ou amarelo claro que é produzido pela oxidação do cério (Ce) pelo oxigênio até sua valência 4+. A fórmula química do óxido cérico é CeOdois e é o óxido de cério mais estável.
O cério (Ce) é um elemento da série dos lantanídeos, que estão incluídos no grupo das terras raras. A fonte natural desse óxido é o mineral bastnasita. No concentrado comercial deste mineral o CeOdois pode ser encontrado em uma proporção aproximada de até 30% em peso.

O CEOdois pode ser facilmente obtido por aquecimento de hidróxido de cério (III), Ce (OH) no ar ou oxigênio3, ou qualquer sal de cério (III), como oxalato, carbonato ou nitrato.
O CEOdois Estequiométrico pode ser obtido pela reação de alta temperatura do óxido de cério (III) com o oxigênio elementar. O oxigênio deve estar em excesso e tempo suficiente deve ser concedido para completar a conversão das várias fases não estequiométricas que estão sendo formadas..
Essas fases compreendem produtos multicoloridos com a fórmula CeOx (onde x varia entre 1,5 e 2,0). Eles também são chamados de CeO2-x, onde x pode ter um valor de até 0,3. O CEOdois É a forma de Ce mais utilizada na indústria. Possui uma classificação de baixa toxicidade, principalmente devido à sua baixa solubilidade em água..

Índice do artigo
- 1 Estrutura
- 2 Nomenclatura
- 3 propriedades
- 3.1 Estado físico
- 3.2 Dureza de Mohs
- 3.3 Peso molecular
- 3.4 Ponto de fusão
- 3,5 Densidade
- 3.6 Solubilidade
- 3.7 Índice de refração
- 3.8 Outras propriedades
- 4 usos
- 4.1 - Na indústria metalúrgica
- 4.2 - Na indústria do vidro
- 4.3 - Em esmaltes
- 4.4 - Em cerâmica zircônia
- 4.5 - Em catalisadores para controle de emissão veicular
- 4.6 - Na catálise de reações químicas
- 4.7 - Em aplicações biológicas e biomédicas
- 4.8 - Outros usos
- 5 referências
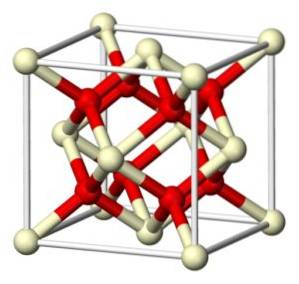
Estrutura
O óxido de cério estequiométrico (IV) cristaliza na estrutura cúbica semelhante a fluorita (CaFdois), com 8 íonsdois- em uma estrutura cúbica coordenada com 4 íons Ce4+.
Nomenclatura
- Óxido de cério (IV).
- Óxido cérico.
- Dióxido de cério.
- Ceria.
- Óxido de cério estequiométrico: material feito inteiramente de CeOdois.
- Óxido de cério não estequiométrico: material formado por óxidos mistos de CeOdois até o CeO1,5
Propriedades
Estado físico
Sólido amarelo pálido. A cor é sensível à estequiometria e à presença de outros lantanídeos. Óxidos não estequiométricos são frequentemente azuis.
Dureza de Mohs
6-6.1 aproximadamente.
Peso molecular
172,12 g / mol.
Ponto de fusão
2600 ºC aproximadamente.
Densidade
7,132 g / cm3
Solubilidade
Insolúvel em água quente e fria. Solúvel em ácido sulfúrico concentrado e ácido nítrico concentrado. Insolúvel em ácidos diluídos.
Índice de refração
2,2.
Outras propriedades
O CEOdois É uma substância inerte, não é atacada por ácidos ou álcalis fortes. No entanto, pode ser dissolvido por ácidos na presença de agentes redutores, como o peróxido de hidrogênio (HdoisOUdois) ou estanho (II), entre outros, gerando soluções de cério (III).
Possui alta estabilidade térmica. Não sofre alterações cristalográficas durante os intervalos de aquecimento usuais.
Seu derivado hidratado (CeOdois.nHdoisO) é um precipitado amarelo e gelatinoso obtido pelo tratamento de soluções de cério (IV) com bases.
O CEOdois é pouco absorvido pelo trato gastrointestinal, por isso não tem efeitos tóxicos.
Formulários
- Na indústria metalúrgica
O CEOdois usado nos eletrodos de certas tecnologias de soldagem, como a soldagem a arco com gás inerte de tungstênio.
O óxido é finamente disperso em toda a matriz de tungstênio. Em baixas tensões, essas partículas CeOdois dar maior confiabilidade do que o tungstênio sozinho.
- Na industria do vidro
Polimento de vidro
O óxido de cério é o agente de polimento mais eficiente para a maioria das composições comerciais de vidro. O CEOdois substituiu quase completamente outros óxidos de polimento, como o FedoisOU3, sílica e ZrOdois, devido à sua maior velocidade de polimento e limpeza, que aumentam conforme o grau de pureza do óxido aumenta.
Os polidores de vidro comerciais baseados em óxido de cério em pó têm tamanhos de partícula definidos e dispersibilidade controlada em sistemas aquosos..
O processo de polimento do vidro requer água e o que é removido ou reformado é uma camada superficial hidratada mais macia. O agente de polimento deve ter uma dureza de Mohs de aproximadamente 6,5, próxima à dureza da maioria dos vidros.
O óxido de cério na água contém o par Ce (IV) / Ce (III) que, com suas reações de oxidação-redução, pode fornecer assistência química durante a quebra da rede de silicato de vidro.
O CEOdois com alto grau de pureza, é utilizado para tratar espelhos, televisores, lentes oftálmicas e materiais óticos de precisão.
Descoloração do vidro
O CEOdois pode descolorir vidros de cal sodada para garrafas, jarros e similares. Ce (IV) oxida as impurezas de Fe (II), que fornecem uma cor verde-azulada, para Fe (III), que dá uma cor amarela 10 vezes mais fraca.
Vidro resistente à radiação
A adição de 1% CeOdois Todo o vidro suprime a descoloração ou escurecimento do vidro causado pelo bombardeio de elétrons de alta energia em vidros de TV. O mesmo é verdadeiro para o vidro usado em janelas de células quentes na indústria nuclear, pois suprime a descoloração induzida por raios gama..
Acredita-se que o mecanismo de supressão dependa da presença de íons Ce4+ e Ce3+ na rede de vidro.
Óculos fotossensíveis
Algumas formulações de vidro podem desenvolver imagens latentes que podem então ser convertidas em uma estrutura ou cor permanente..
Este tipo de vidro contém CeOdois que absorve a radiação UV e libera elétrons na matriz de vidro.
Após o tratamento, o crescimento de cristais de outros compostos no vidro é gerado, criando padrões detalhados para usos eletrônicos ou decorativos..
- Em esmaltes
Devido ao seu alto índice de refração, CeOdois é um agente opacificante em composições de esmalte usado como revestimentos protetores em metais.
A sua elevada estabilidade térmica e a sua forma cristalográfica única em toda a gama de temperaturas atingidas durante o processo de esmaltação, tornam-no adequado para utilização em esmaltes de porcelana..
Neste aplicativo o CeOdois Fornece o revestimento branco desejado durante a queima do esmalte. É o ingrediente que fornece opacidade.
- Em cerâmica de zircônio
A cerâmica de zircônio é um isolante térmico e é usada em aplicações de alta temperatura. Requer um aditivo para ter alta resistência e tenacidade. Adicionando CeOdois O óxido de zircônio produz um material com excepcional tenacidade e boa resistência.
Óxido de zircônio dopado com CeOdois usado em revestimentos para atuar como uma barreira térmica em superfícies de metal.
Por exemplo, em peças de motores de aeronaves, esses revestimentos protegem das altas temperaturas às quais os metais seriam expostos..
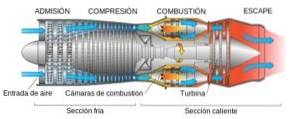
- Em catalisadores para controle de emissão de veículos
O CEOdois É um componente ativo na remoção de poluentes das emissões veiculares. Isso se deve em grande parte à sua capacidade de armazenar ou liberar oxigênio, dependendo das condições ao seu redor..
O conversor catalítico em veículos motorizados está localizado entre o motor e a saída dos gases de escape. Tem um catalisador que deve oxidar hidrocarbonetos não queimados, converter CO em COdois, e reduzir os óxidos de nitrogênio, NOx, toneladadois Eudois.

Além da platina e de outros metais catalíticos, o principal componente ativo desses sistemas multifuncionais é o CeOdois.
Cada conversor catalítico contém 50-100 g de CeOdois finamente dividido, que cumpre várias funções. Os mais importantes são:
Atua como um estabilizador para alumina de alta área de superfície
A alumina de alta área superficial tende a sinterizar, perdendo sua alta área superficial durante a operação em alta temperatura. Isso é atrasado pela presença de CeOdois.
Ele se comporta como um liberador de buffer de oxigênio
Devido à sua capacidade de formar óxidos não estequiométricos CeO2-x, óxido de cério (IV) fornece oxigênio elementar de sua própria estrutura durante o período do ciclo pobre de oxigênio / rico em combustível.
Assim, a oxidação de hidrocarbonetos não queimados vindos do motor e a conversão de CO em CO podem continuar.dois, mesmo quando o oxigênio gasoso é insuficiente.
Então, no período do ciclo rico em oxigênio, ele pega o oxigênio e se reoxida, recuperando sua forma estequiométrica CeOdois.
Outras
Atua como potencializador da capacidade catalítica do ródio na redução dos óxidos de nitrogênio NOx para nitrogênio e oxigênio.
- Na catálise de reações químicas
Nos processos de craqueamento catalítico de refinarias, CeOdois atua como um oxidante catalítico que auxilia na conversão de SOdois para então3 e promove a formação de sulfatos em armadilhas específicas do processo.
O CEOdois melhora a atividade do catalisador à base de óxido de ferro usado para obter estireno a partir do etilbenzeno. Isso possivelmente se deve à interação positiva entre os pares óxido-redução Fe (II) - Fe (III) e Ce (III) - Ce (IV).
- Em aplicações biológicas e biomédicas
Nanopartículas de CeO foram encontradasdois funcionam eliminando radicais livres, como superóxido, peróxido de hidrogênio, hidroxila e radical de óxido nítrico.
Eles podem proteger os tecidos biológicos de danos induzidos por radiação, danos retinais induzidos por laser, aumentar a expectativa de vida das células fotorreceptoras, reduzir lesões na coluna, reduzir a inflamação crônica e promover angiogênese ou formação de vasos sanguíneos.
Além disso, certas nanofibras contendo nanopartículas de CeOdois têm se mostrado tóxicos contra cepas bacterianas, sendo candidatos promissores para aplicações bactericidas.
- Outros usos
O CEOdois É um isolante elétrico devido à sua excelente estabilidade química, alta permissividade relativa (tem alta tendência a polarizar quando um campo elétrico é aplicado) e uma rede cristalina semelhante ao silício..
Encontrou aplicação em capacitores e camadas de amortecimento de materiais supercondutores.
Ele também é usado em sensores de gás, materiais de eletrodo de célula de combustível de óxido sólido, bombas de oxigênio e monitores de oxigênio..
Referências
- Cotton, F. Albert e Wilkinson, Geoffrey. (1980). Química Inorgânica Avançada. Quarta edição. John Wiley & Sons.
- Bailar, J.C.; Emeléus, H.J.; Sir Ronald Nyholm e Trotman-Dickenson, A.F. (1973). Comprehensive Inorganic Chemistry. Volume 4. Pergamon Press.
- Kirk-Othmer (1994). Enciclopédia de Tecnologia Química. Volume 5. Quarta Edição. John Wiley & Sons.
- Enciclopédia de Química Industrial de Ullmann. (1990). Quinta edição. Volume A6. VCH Verlagsgesellschaft mbH.
- Casals, Eudald et al. (2012). Análise e Risco de Nanomateriais em Amostras Ambientais e Alimentares. Em Comprehensive Analytical Chemistry. Recuperado de sciencedirect.com.
- Mailadil T. Sebastian. (2008). Alumina, Titânia, Ceria, Silicato, Tungstate e outros materiais. Em materiais dielétricos para comunicação sem fio. Recuperado de sciencedirect.com.
- Afeesh Rajan Unnithan, et al. (2015). Andaimes com propriedades antibacterianas. Em Aplicações de Nanotecnologia para Engenharia de Tecidos. Recuperado de sciencedirect.com.
- Gottardi V., et al. (1979). Polir a superfície de um vidro investigado com uma técnica nuclear. Boletim da Sociedade Espanhola de Cerâmica e Vidro, Vol. 18, No. 3. Recuperado de boletines.secv.es.



Ainda sem comentários