
Biografia de Gilbert Newton Lewis e contribuições para a ciência
Gilbert Newton Lewis Ele foi um dos cientistas americanos mais importantes do século XX. Seu trabalho produziu uma revolução estrutural nos estudos químicos, graças às muitas contribuições que ele fez ao longo de sua vida para o desenvolvimento da ciência..
Dentre as contribuições desse físico-químico, destaca-se a fórmula que leva seu nome, com a qual apenas os pares de elétrons são representados graficamente. O trabalho de pesquisa de Lewis foi muito extenso, embora sua fama se devesse basicamente à teoria sobre ligações químicas e à definição de ácido-base formulada em 1923.

Lewis passou a ter grande influência no mundo científico e acadêmico dos Estados Unidos, especialmente na Universidade de Harvard, onde treinou e ensinou. Seu trabalho para o Exército dos Estados Unidos durante a Primeira Guerra Mundial rendeu-lhe o maior reconhecimento e as mais altas honras..
Ele treinou nas universidades de Nebraska, Harvard, Leipzig e Göttingen na Alemanha. Ele trabalhou no Massachusetts Institute of Technology (MIT), na Harvard University e na University of California, onde morreu trabalhando.
Ao longo de sua vida, ele recebeu inúmeros reconhecimentos e prêmios, incluindo vários doutorados honorários das universidades de Chicago, Madrid, Liverpool, Wisconsin e Pensilvânia. Ele foi membro honorário de várias instituições científicas na Inglaterra, Índia, Suécia, Dinamarca e Estados Unidos..
Índice do artigo
- 1 biografia
- 1.1 Estudos
- 1.2 Trabalho acadêmico e participação na guerra
- 1.3 Morte em laboratório
- 2 contribuições para a ciência
- 2.1 Estruturas de Lewis
- 2.2 Ligação covalente
- 2.3 Teoria do octeto
- 2,4 Photon
- 2.5 Atração química e valência
- 2.6 Água pesada
- 2.7 Teoria das soluções
- 3 referências
Biografia
Gilbert Newton Lewis nasceu em Weymouth, Massachusetts, em 23 de outubro de 1875. Seus pais eram Frank Wesley Lewis e Mary Burr White Lewis. Durante seus primeiros anos, ele foi ensinado em sua própria casa e aos 10 anos entrou na escola pública, formando-se em 1889.
Em 1884, Lewis teve que se estabelecer com sua família em Lincoln, Nebraska. Aos 13 anos, ele foi admitido na University of Nebraska High School..
Estudos
Após a formatura, ele prosseguiu seus estudos universitários por dois anos e, em seguida, matriculou-se na Universidade de Harvard em 1893.
Inicialmente ele se interessou por economia, mas acabou optando por física e química. Gilbert se formou em química em 1896 e por um ano ele lecionou na Phillips Academy, uma escola particular em Andover..
Ele voltou a Harvard para trabalho de pós-graduação e mestrado em 1898 com sua tese sobre O elétron e uma molécula. Um ano depois, ele obteve o doutorado e sua tese foi intitulada Algumas relações eletroquímicas e termoquímicas de amálgamas de zinco e cádmio".
Em Harvard, ele serviu como instrutor por um ano, depois viajou para a Europa com uma bolsa de estudos. Ele estudou com os grandes físico-químicos da época.
Em 1899 ele viajou para a Alemanha para estudar com Wilhelm Ostwald Leipzig e mais tarde com Walter Nernst na Universidade de Göttingen; então ele trabalhou para o governo filipino.
Trabalho acadêmico e participação na guerra
Entre 1999 e 1906 ele ensinou química na Universidade de Harvard e mais tarde foi contratado pelo Instituto de Tecnologia de Massachusetts, onde foi de 1907 a 1912.
Mais tarde, ele se tornou professor de físico-química na Universidade da Califórnia (Berkeley), onde obteve o título de reitor da Escola de Química..
Em 1908, ele publicou seu primeiro artigo sobre a teoria da relatividade em paralelo com Albert Einstein. Nisto ele estabelece que existe uma ligação entre energia-massa, mas em uma direção diferente daquela usada por Einstein..
Em 21 de junho de 1912, Lewis casou-se com Mary Hinckley Sheldon, com quem teve três filhos: Margery S. Lewis, Edward S. Lewis e Richard Newton Lewis..
Seu trabalho na Califórnia foi interrompido pela eclosão da Primeira Guerra Mundial. Em 1917, ele foi contratado para trabalhar para o Exército dos Estados Unidos, onde se tornou chefe da Divisão de Defesa do Serviço de Guerra Química..
A dedicação e capacidade de trabalho de Lewis permitiram ao exército reduzir o número de baixas que havia sofrido até então como resultado do uso de gás pelos exércitos inimigos. No final da guerra, ele recebeu as maiores honras por seus serviços.
Morte no laboratório
Gilbert N. Lewis morreu aos 70 anos de ataque cardíaco enquanto trabalhava em seu laboratório na Universidade de Berkeley, em 23 de março de 1946..
Talvez devido à sua personalidade introvertida, este eminente cientista nunca recebeu o Prêmio Nobel. Quase no final da carreira, conseguiu provar que a fosforescência das moléculas orgânicas é governada por um estado de tripleto excitado, chegando até a calcular suas propriedades magnéticas..
Contribuições para a ciência
Algumas das contribuições mais importantes de Gilbert Newton Lewis para a ciência são as seguintes:
Estruturas de Lewis
Existem vários métodos que servem para representar a estrutura de uma molécula. Nestes, os símbolos dos elementos representam os átomos, enquanto os pontos representam os elétrons que os rodeiam. Um exemplo disso é a representação de hidrogênio, hélio e carbono:
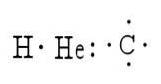
Lewis foi o primeiro a ter a ideia de que os átomos podiam permanecer juntos comparando pares de elétrons; é por isso que ele criou o simbolismo das estruturas.
A teoria da ligação ampla proposta por Lewis serviu para agrupar em um único conceito todos os tipos de ligações químicas. Desta forma foi possível demonstrar as relações entre as substâncias iônicas, moleculares, covalentes e metálicas. Até aquele momento, esses elementos não tinham nenhuma conexão conceitual..
Ligação covalente
Ele conceituou a ligação covalente que se forma entre dois átomos quando se unem para atingir o octeto estável e compartilham elétrons do último nível, exceto para o hidrogênio, que consegue alcançar estabilidade por ter 2 elétrons.
Teoria do octeto
Foi enunciado por Lewis em 1916. Nele se estabelece que os íons pertencentes aos elementos do sistema periódico tendem a completar seus últimos níveis de energia com um número de 8 elétrons. Isso permite que eles adquiram uma configuração muito estável.
Fóton
Ele foi o criador em 1926 do termo fóton para designar a menor unidade de energia luminosa. Esta partícula de energia transmite todas as formas existentes de radiação eletromagnética (raios X, infravermelho, gama, ultravioleta, microondas, ondas de rádio, etc.).
Atração química e valência
Junto com seu colega químico Irwing Langmuir, ele desenvolveu a teoria da atração química e valência, conhecida como teoria de Langmuir-Lewis. Para isso, ele confiou na estrutura atômica das substâncias.
Água pesada
Lewis também foi o primeiro cientista a estudar e produzir água pesada (deutério) em seu estado puro. Ele também foi o primeiro a aplicar os princípios da termodinâmica no estudo de problemas químicos..
Teoria da solução
Da mesma forma, Lewis é reconhecido por seu trabalho na teoria das soluções; ou seja, as misturas homogêneas que são obtidas a partir da interposição de átomos, moléculas ou íons presentes em duas ou mais substâncias. Essas substâncias chamadas componentes estão envolvidas em proporções variáveis.
Referências
- Gilbert Newton Lewis (1875-1946). Academia Nacional de Ciências (PDF). Consultado de nasonline.org.
- Historical Figures in Chemistry: Gilbert Newton Lewis (1875-1946). Consultado de uv.es
- Gilbert Newton Lewis. Consultado de historia-biografia.com
- Gilbert Newton Lewis. Consultado de biografiasyvidas.com
- Biografia de Gilbert N. Lewis. Consultado por biografias.wiki
- 7 coisas que você realmente precisa saber sobre Gilbert Newton Lewis, o cientista que quase derrotou Einstein. Consultado de vix.com
- Gilbert Lewis e o centenário da teoria das ligações de pares de elétrons (Parte 1). Consultado de bicsociety.org



Ainda sem comentários