
Estrutura, propriedades, produção e usos do ácido maleico

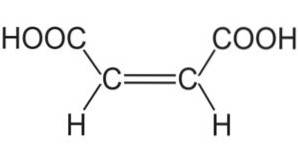
O ácido maleico é um composto orgânico ácido cuja fórmula química é HOOC-CH = CH-COOH. É um ácido dicarboxílico. Também é conhecido como ácido cis-butenodioico, ácido maleínico, ácido malênico e ácido toxílico.
O ácido maleico é encontrado naturalmente no tabaco, ginseng e bebidas como cerveja e vinho. Também é encontrado na fumaça do cigarro e no escapamento de automóveis.
Sua ligação dupla e os dois grupos -COOH o tornam suscetível a várias reações químicas, razão pela qual é usado para sintetizar muitos outros compostos, materiais e produtos..
Também é de grande ajuda para o processamento de tecidos como algodão, lã e seda. Permite obter colas, resinas e óleos sintéticos. É usado para prevenir a oxidação de gorduras e óleos. Por sua vez, muitos de seus derivados são usados em aplicações médicas e veterinárias..
Segundo algumas pesquisas, é um dos componentes das bebidas fermentadas que estimula a secreção de ácido gástrico.
Índice do artigo
- 1 Estrutura
- 2 Nomenclatura
- 3 propriedades
- 3.1 Estado físico
- 3.2 Peso molecular
- 3.3 Ponto de fusão
- 3.4 Ponto de ebulição
- 3.5 Peso específico
- 3.6 Solubilidade
- 3.7 Constantes de dissociação
- 3.8 Propriedades químicas
- 4 Obtendo
- 5 usos do ácido maleico
- 5.1 Na produção de outros compostos químicos
- 5.2 Em várias aplicações
- 5.3 Na indústria têxtil
- 5.4 Na medicina
- 5.5 Em odontologia
- 5.6 Em medicina veterinária
- 5.7 Uso potencial como desinfetante
- 6 Efeitos do ácido maleico contido em bebidas fermentadas, como cerveja e vinho
- 7 riscos
- 8 referências
Estrutura
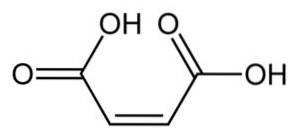
A molécula de ácido maleico é formada por um esqueleto de 4 átomos de carbono, dos quais as duas extremidades formam grupos carboxila -COOH e as duas centrais formam uma ligação dupla C = C..
Os grupos -COOH estão localizados na posição cis no que diz respeito à ligação dupla. Os oxigênios e hidrogênios do -COOH são acomodados de tal forma que um hidrogênio está localizado entre os oxigênios..
Nomenclatura
- Ácido maleico
- Ácido cis-butenodioico
- Ácido toxílico
- Ácido maleínico
- Ácido maleico
Propriedades
Estado físico
Sólido cristalino incolor, cristais monoclínicos.

Peso molecular
116,07 g / mol
Ponto de fusão
130,5 ºC
Ponto de ebulição
135 ºC (decompõe-se)
Peso específico
1.609
Solubilidade
Muito solúvel em água: 79 g / 100 g HdoisOu a 20 ºC
Constantes de dissociação
K1 = 1000 x 10-5
Kdois = 0,055 x 10-5
Propriedades quimicas
O ácido maleico tem dois grupos -COOH e uma ligação dupla C = C central como locais reativos.
Seu anidrido é uma molécula cíclica de 5 átomos, cujos produtos são instáveis à hidrólise, principalmente os produtos da reação com grupos amino -NHdois.
Isso o torna um bloqueador reversível de grupos -NH.dois para mascará-los temporariamente e evitar que reajam quando outras reações estiverem ocorrendo.
Isso é útil para vários fins, especialmente para modificar proteínas em nível de laboratório..
Obtendo
Industrialmente, é obtido pela oxidação catalítica do benzeno na presença de pentóxido de vanádio..
Também por oxidação de n-butano ou n-butileno na fase de vapor com ar, na presença de um catalisador sólido.
Também pode ser obtido pela hidrólise do anidrido maleico.
Também é obtido como subproduto da fabricação do anidrido ftálico a partir do naftaleno..
Uso de ácido maleico
Na produção de outros compostos químicos
O ácido maleico permite a obtenção de muitos outros compostos químicos. É utilizado na síntese de ácido aspártico, málico, tartárico, succínico, lático, malônico, propiônico e acrílico.
Como um intermediário químico, o ácido maleico é usado em quase todos os campos da química industrial..
Em várias aplicações
O ácido maleico permite a obtenção de colas sintéticas, corantes, resinas alquídicas e óleos sintéticos.
Seus derivados, os sais maleato, são usados em formulações de anti-histamínicos e medicamentos semelhantes..
É usado como conservante em gorduras e óleos, pois serve para retardar o aparecimento de ranço.
É usado em inibidores de corrosão e produtos anti-incrustantes. Também funciona como um agente regulador do pH.
Na industria textil
É utilizado no processamento de lã, seda e algodão.
A obtenção de oligômeros (polímeros de poucas unidades) de ácido maleico tem sido investigada para utilizá-los como agente de acabamento na obtenção de algodão prensado permanente, de forma a não utilizar polímeros de formaldeído..
Neste caso, a polimerização do ácido maleico é realizada em meio aquoso na presença de NaHdoisPOdois e um iniciador radical como NadoisSdoisOU8. O oligômero de ácido maleico tem grupos carboxila -COOH ligados ao -CHdois- partes adjacentes do seu esqueleto molecular.
É aplicado ao tecido de algodão como um agente formador de rede e o processo de cura é realizado.
Assim, o oligômero de ácido maleico é eficaz na reticulação da celulose do algodão e conferindo altos níveis de resistência ao enrugamento aos tecidos de algodão..
Além disso, os tecidos tratados com polímeros de ácido maleico não apresentaram amarelecimento e apresentaram maior retenção de força ou resistência do que aqueles tratados com polímeros de formaldeído..

Em medicina
Existem vários compostos à base de ácido maleico que são usados no tratamento do câncer.
O maleato de sunitinibe (Sutent) é um medicamento anticâncer que atua de várias maneiras para inibir a proliferação de células tumorais e a angiogênese..
É aprovado para o tratamento de carcinoma de células renais e tumor gastrointestinal resistente a medicamentos. Sua atividade no carcinoma hepatocelular e no câncer de células do pulmão está sendo investigada. Fornecido por via oral em cápsulas.
De acordo com um estudo realizado em 2015, nanopartículas foram preparadas com um copolímero de estireno-ácido maleico ao qual o medicamento Paclitaxel usado no tratamento do câncer foi ligado por meio de uma ligação éster..
Essas nanopartículas apresentaram maior retenção no plasma e no tumor, inibindo o crescimento deste com melhora no efeito de apoptose (morte) das células cancerosas..
Não apresentaram toxicidade nos principais órgãos, tecidos e sistema hematológico.
Por estas razões, eles são propostos como um sistema alternativo de entrega ou entrega de drogas em tumores sólidos.
Na odontologia
De acordo com algumas pesquisas, o ácido maleico a 10% reduz a perda mineral dos dentes quando aplicado em tratamentos dentários.
É usado para corroer suavemente a superfície do dente e, assim, promover a adesão de outros materiais.
É relatado que pode produzir forças de ligação ou adesão iguais às do ácido ortofosfórico a 37%.
Na medicina veterinária
O maleato de accepromazina é usado como tranquilizante em medicina veterinária para sedação de animais antes da anestesia. Este composto protege contra os efeitos da anestesia geradores de arritmia.
Uso potencial como desinfetante
Foi descoberto recentemente (2018) que o ácido maleico pode inibir a resistência das bactérias Listeria monocytogenes a ácidos tornando-o suscetível à ação destes quando são usados para desinfetar na indústria alimentícia.
Acredita-se que atue sobre uma enzima que favorece a resistência desses microrganismos aos ácidos, desativando-a. O ácido maleico também demonstrou remover biofilmes dessas bactérias..
Essas características o tornam um candidato potencial para desinfecção de equipamentos na indústria de alimentos..
Efeitos do ácido maleico contido em bebidas fermentadas, como cerveja e vinho
Estudos conduzidos com humanos que ingeriram soluções fermentadas de glicose descobriram que os ácidos dicarboxílicos, como o ácido maleico, são estimulantes do ácido gástrico poderosos.
Segundo os pesquisadores, isso é muito provável de ocorrer no caso de bebidas fermentadas como cerveja, champanhe e vinho, mas não em bebidas alcoólicas destiladas como whisky e conhaque..
Isso ocorre porque o efeito estimulante do ácido gástrico é causado por ácidos dicarboxílicos, como o ácido maleico, e não pelo álcool (etanol).
Riscos
O contato do ácido maleico com os olhos ou a pele causa irritação e pode causar dermatite por contato prolongado. A inalação causa irritação no nariz e na garganta. Pode ter um efeito prejudicial nos rins.
Quando exposto ao calor ou chama, ocorre sua combustão e os gases ou fumos produzidos causam irritação..
Se o ácido maleico for liberado, espera-se que o ambiente seja quebrado ou decomposto por microorganismos. Não se acumula em organismos aquáticos.
Referências
- NÓS. Biblioteca Nacional de Medicina. (2019). Ácido maleico. Recuperado de: pubchem.ncbi.nlm.nih.gov.
- Hermanson, G.T. (2013). Alvos funcionais para bioconjugação. In Bioconjugate Techniques (Third Edition). Recuperado de sciencedirect.com.
- Teyssen, S. et al. (1999). O ácido maleico e o ácido succínico nas bebidas alcoólicas fermentadas são os estimulantes da secreção de ácido gástrico. J. Clin. Investir. 1999; 103 (5): 707-713. Recuperado de jci.org.
- Flecknell, P. et al. (2015). Pré-anestesia, anestesia, analgesia e eutanásia. Em Laboratory Animal Medicine (terceira edição). Recuperado de sciencedirect.com.
- Chen, D. et al. (2005). Polimerização Aquosa do Ácido Maleico e Cross-Linking da Celulose do Algodão por Poli (ácido maleico). Ind. Eng. Chem. Res. 2005, 44, 7921-7927. Recuperado de pubs.acs.org.
- Carver, J.R. (2011). Gerenciamento de efeitos colaterais relacionados ao tratamento cardíaco e pulmonar. In Supportive Oncology. Recuperado de sciencedirect.com.
- SerdarÜsümez, NejatErverdi. (2010). Adesivos e Colagem em Ortodontia. Em Terapia Atual em Ortodontia. Recuperado de sciencedirect.com.
- Dalela, M. et al. (2015). Nanopartículas biocompatíveis sensíveis ao pH de poli (ácido estireno-co-maleico) conjugado com paclitaxel para a administração de drogas anticâncer em tumores sólidos de camundongos singênicos. Interfaces ACS Appl Mater. 9 de dezembro de 2015; 7 (48): 26530-48. Recuperado de ncbi.nlm.nih.gov.
- Paudyal, R. et al. (2018). Uma nova abordagem em desinfecção ácida através da inibição de mecanismos resistentes a ácidos; A inibição mediada pelo ácido maleico da atividade da glutamato descarboxilase aumenta a sensibilidade ao ácido de Listeria monocytogenes. Food Mycrobiol. 69: 96-104 de fevereiro de 2018. Recuperado de ncbi.nlm.nih.gov.



Ainda sem comentários