
Formação, propriedades e aplicações de sais de diazônio
As sais de diazônio são compostos orgânicos nos quais existem interações iônicas entre o grupo azo (-Ndois+) e um ânion X- (Cl-, F-, CH3COO-, etc.). Sua fórmula química geral é RNdois+X-, e nesta a cadeia lateral R pode bem ser um grupo alifático ou um grupo arilo; ou seja, um anel aromático.
A imagem inferior representa a estrutura do íon arenediazônio. As esferas azuis correspondem ao grupo azo, enquanto as esferas pretas e brancas compõem o anel aromático do grupo fenil. O grupo azo é muito instável e reativo, porque um dos átomos de nitrogênio tem uma carga positiva (-N+≡N).
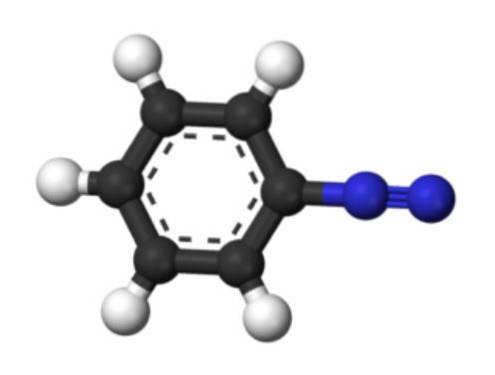
No entanto, existem estruturas de ressonância que deslocalizam esta carga positiva, por exemplo, no átomo de nitrogênio vizinho: -N = N+. Isso se origina quando um par de elétrons formando uma ligação vai para o átomo de nitrogênio à esquerda.
Da mesma forma, essa carga positiva pode ser deslocalizada pelo sistema Pi do anel aromático. Como consequência, os sais de diazônio aromáticos são mais estáveis do que os alifáticos, uma vez que a carga positiva não pode ser deslocalizada ao longo de uma cadeia de carbono (CH3, CHdoisCH3, etc.).
Índice do artigo
- 1 treinamento
- 2 propriedades
- 2.1 Reações de deslocamento
- 2.2 Outros deslocamentos
- 2.3 Reações Redox
- 2.4 Decomposição fotoquímica
- 2,5 reações de acoplamento Azo
- 3 aplicativos
- 4 referências
Treinamento
Estes sais são derivados da reação de uma amina primária com uma mistura ácida de nitrito de sódio (NaNOdois).
Aminas secundárias (RdoisNH) e terciário (R3N) originam outros produtos nitrogenados, como N-nitrosoaminas (que são óleos amarelados), sais de amina (R3HN+X-) e compostos de N-nitrosoamônio.
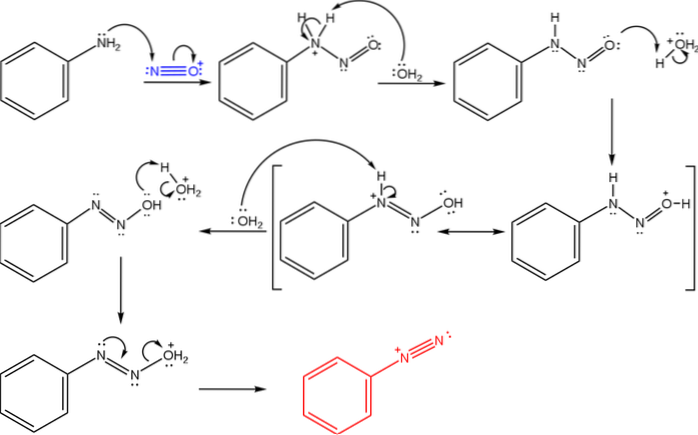
A imagem superior ilustra o mecanismo pelo qual a formação de sais de diazônio é governada, ou também conhecida como reação de diazotização..
A reação começa com fenilamina (Ar-NHdois), que realiza um ataque nucleofílico ao átomo N do cátion nitrosônio (NO+) Este cátion é produzido pela mistura NaNOdois/ HX, onde X é geralmente Cl; ou seja, HCl.
A formação do cátion nitrosônio libera água no meio, que remove um próton do nitrogênio carregado positivamente..
Então, esta mesma molécula de água (ou outra espécie ácida diferente de H3OU+) produz um próton para o oxigênio, deslocando a carga positiva no átomo de nitrogênio menos eletronegativo).
Agora, a água novamente desprotona o nitrogênio, produzindo assim a molécula de diazo-hidróxido (o penúltimo na sequência).
Como o meio é ácido, o diazohidróxido sofre desidratação do grupo OH; para neutralizar a vacância eletrônica, o par livre de N forma a ligação tripla do grupo azo.
Assim, ao final do mecanismo, o cloreto de benzenediazônio (C6H5Ndois+Cl-, o mesmo cátion da primeira imagem).
Propriedades
Em geral, os sais de diazônio são incolores e cristalinos, solúveis e estáveis em baixas temperaturas (menos de 5 ºC)..
Alguns desses sais são tão sensíveis ao impacto mecânico que qualquer manipulação física poderia detoná-los. Finalmente, eles reagem com água para formar fenóis.
Reações de deslocamento
Os sais de diazônio são liberadores potenciais de nitrogênio molecular, cuja formação é o denominador comum nas reações de deslocamento. Nestes, uma espécie X desloca o grupo azo instável, escapando como Ndois(g).
Reação de Sandmeyer
ArNdois+ + CuCl => ArCl + Ndois + Cu+
ArNdois+ + CuCN => ArCN + Ndois + Cu+
Reação do Gatterman
ArNdois+ + CuX => ArX + Ndois + Cu+
Ao contrário da reação de Sandmeyer, a reação de Gatterman tem cobre metálico no lugar de seu haleto; ou seja, o CuX é gerado no local.
Reação de Schiemann
[ArNdois+] BF4- => ArF + BF3 + Ndois
A reação de Schiemann é caracterizada pela decomposição térmica do fluoroborato de benzenediazônio..
Reação de Gomberg Bachmann
[ArNdois+] Cl- + C6H6 => Ar - C6H5 + Ndois + HCl
Outros deslocamentos
ArNdois+ + KI => ArI + K+ + Ndois
[ArNdois+] Cl- + H3POdois + HdoisO => C6H6 + Ndois + H3PO3 + HCl
ArNdois+ + HdoisO => ArOH + Ndois + H+
ArNdois+ + Carimbodois => ArNOdois + Ndois + Cu+
Reações redox
Os sais de diazônio podem ser reduzidos a arilhidrazinas, usando uma mistura de SnCldois/ HCl:
ArNdois+ => ArNHNHdois
Eles também podem ser reduzidos a arilaminas em reduções mais fortes com Zn / HCl:
ArNdois+ => ArNHdois + NH4Cl
Decomposição fotoquímica
[ArNdois+] X- => ArX + Ndois
Os sais de diazônio são sensíveis à decomposição pela incidência de radiação ultravioleta ou em comprimentos de onda muito próximos.
Reações de acoplamento azo
ArNdois+ + Ar'H → ArNdoisAr '+ H+
Essas reações são talvez as mais úteis e versáteis dos sais de diazônio. Esses sais são eletrófilos fracos (o anel desloca a carga positiva do grupo azo). Para que reajam com compostos aromáticos, eles precisam ser carregados negativamente, dando origem a compostos azos..
A reação ocorre com rendimento eficiente entre pH 5 e 7. Em pH ácido o acoplamento é menor porque o grupo azo é protonado, impossibilitando o ataque ao anel negativo..
Da mesma forma, em pH básico (maior que 10), o sal de diazônio reage com o OH- para produzir diazohidróxido, que é relativamente inerte.
As estruturas desse tipo de composto orgânico possuem um sistema Pi conjugado muito estável, cujos elétrons absorvem e emitem radiação no espectro visível..
Consequentemente, os compostos azo são caracterizados por serem coloridos. Devido a esta propriedade, eles também são chamados de corantes azo..
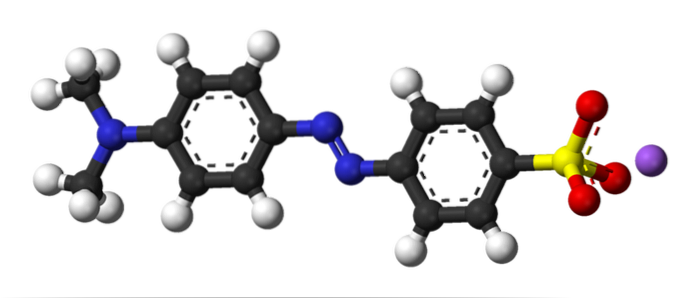
A imagem acima ilustra o conceito de acoplamento azo com laranja de metila como exemplo. No meio de sua estrutura, o grupo azo pode ser visto servindo como o conector dos dois anéis aromáticos.
Qual dos dois anéis era o eletrófilo no início do acoplamento? O da direita, porque o grupo sulfonato (-SO3) remove a densidade de elétrons do anel, tornando-o ainda mais eletrofílico.
Formulários

Uma de suas aplicações mais comerciais é a produção de corantes e pigmentos, abrangendo também a indústria têxtil no tingimento de tecidos. Esses compostos azo se ancoram em locais moleculares específicos no polímero, colorindo-o.
Devido à sua decomposição fotolítica, é (menos do que antes) utilizado na reprodução de documentos. Como? As áreas do papel recobertas por um plástico especial são removidas e, em seguida, é aplicada uma solução básica de fenol, colorindo as letras ou o desenho de azul..
Em sínteses orgânicas, eles são usados como pontos de partida para muitos derivados aromáticos.
Finalmente, eles estão tendo aplicações na área de materiais inteligentes. Nestes, eles são covalentemente ligados a uma superfície (ouro, por exemplo), permitindo-lhe dar uma resposta química a estímulos físicos externos..
Referências
- Wikipedia. (2018). Composto de diazônio. Obtido em 25 de abril de 2018, em: en.wikipedia.org
- Francis A. Carey. Quimica Organica. Ácidos carboxílicos. (sexta edição, páginas 951-959). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. Química orgânica. Aminas. (10ª edição, páginas 935-940). Wiley plus.
- Clark J. (2016). Reações de sais de diazônio. Obtido em 25 de abril de 2018, em: chemguide.co.uk
- BYJU'S. (05 de outubro de 2016). Sais de diazônio e suas aplicações. Obtido em 25 de abril de 2018, em: byjus.com
- TheGlobalTutors. (2008-2015). Propriedades dos sais de diazônio. Obtido em 25 de abril de 2018 em: theglobaltutors.com
- Ahmad et al. (2015). Polímero. Obtido em 25 de abril de 2018, em: msc.univ-paris-diderot.fr
- CytochromeT. (15 de abril de 2017). Mecanismo de formação do íon benzenediazônio. Obtido em 25 de abril de 2018, em: commons.wikimedia.org
- Jacques Kagan. (1993). Fotoquímica Orgânica: Princípios e Aplicações. Academic Press Limited, página 71. Obtido em 25 de abril de 2018, em: books.google.co.ve


Ainda sem comentários