
Características dos biofilmes, formação, tipos e exemplos
O biofilmes ou biofilmes Eles são comunidades de microrganismos aderidos a uma superfície, vivendo em uma matriz autogerada de substâncias poliméricas extracelulares. Eles foram inicialmente descritos por Antoine von Leeuwenhoek, quando examinou os "animálculos" (assim chamados por ele), em uma placa de material de seus próprios dentes no século XVII..
A teoria que conceitua biofilmes e descreve seu processo de formação não havia sido desenvolvida até 1978. Foi descoberto que a capacidade dos microrganismos de formar biofilmes parece ser universal..
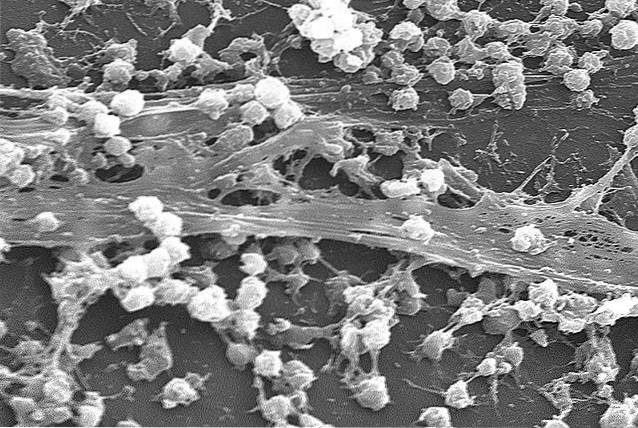
Os biofilmes podem existir em ambientes tão variados como sistemas naturais, aquedutos, tanques de armazenamento de água, sistemas industriais, bem como em uma ampla variedade de meios como dispositivos médicos e dispositivos para permanência em pacientes hospitalares (como cateteres, por exemplo).
Através do uso de microscopia eletrônica de varredura e microscopia confocal a laser de varredura, descobriu-se que os biofilmes não são depósitos de células homogêneos e não estruturados e sedimentos acumulados, mas sim estruturas heterogêneas complexas..
Biofilmes são comunidades complexas de células associadas em uma superfície, encerradas em uma matriz polimérica altamente hidratada cuja água circula por canais abertos da estrutura..
Muitos organismos que tiveram sucesso em sua sobrevivência de milhões de anos no meio ambiente, por exemplo, espécies do gênero Pseudomonas Y Legionella, usar a estratégia de biofilme em ambientes diferentes de seus ambientes nativos nativos.
Índice do artigo
- 1 Características dos biofilmes
- 1.1 Características químicas e físicas da matriz do biofilme
- 1.2 Características ecofisiológicas de biofilmes
- 2 Formação de biofilme
- 2.1 Adesão inicial à superfície
- 2.2 Formação de uma monocamada e microcolônias em multicamadas
- 2.3 Produção da matriz extracelular polimérica e maturação do biofilme tridimensional
- 3 tipos de biofilmes
- 3.1 Número de espécies
- 3.2 Ambiente de treinamento
- 3.3 Tipo de interface onde são gerados
- 4 Exemplos de biofilmes
- 4.1 - Placa dentária
- 4.2 - Biofilmes em água negra
- 4.3 - biofilmes subaeriais
- 4.4 -Biofilmes de agentes causadores de doenças humanas
- 4.5 - Peste Bubônica
- 4.6 - Cateteres venosos hospitalares
- 4.7 - Na indústria
- 5 Resistência de biofilmes a desinfetantes, germicidas e antibióticos
- 6 referências
Características do biofilme
Características químicas e físicas da matriz do biofilme
-Substâncias extracelulares poliméricas secretadas por microrganismos de biofilme, macromoléculas polissacarídicas, proteínas, ácidos nucléicos, lipídios e outros biopolímeros, principalmente moléculas altamente hidrofílicas, cruzam-se para formar uma estrutura tridimensional chamada matriz de biofilme..
-A estrutura da matriz é altamente viscoelástica, possui propriedades de borracha, é resistente à tração e quebras mecânicas.
-A matriz tem a capacidade de aderir a superfícies de interface, incluindo espaços internos de meios porosos, por meio de polissacarídeos extracelulares que atuam como gomas aderentes..
-A matriz polimérica é predominantemente aniônica e também inclui substâncias inorgânicas, como cátions metálicos..
-Possui canais de água por onde circulam oxigênio, nutrientes e substâncias residuais que podem ser recicladas..
-Essa matriz do biofilme funciona como meio de proteção e sobrevivência contra ambientes adversos, uma barreira contra invasores fagocíticos e contra a entrada e difusão de desinfetantes e antibióticos..
Características ecofisiológicas de biofilmes
-A formação da matriz em gradientes não homogêneos produz uma variedade de microhabitats, o que permite que a biodiversidade exista dentro do biofilme..
-Dentro da matriz, a forma de vida celular é radicalmente diferente da vida livre e não associada. Os microrganismos do biofilme são imobilizados, muito próximos uns dos outros, associados em colônias; este fato permite que interações intensas ocorram.
-As interações entre os microrganismos no biofilme incluem a comunicação por meio de sinais químicos em um código chamado "quorum sensing"..
-Existem outras interações importantes, como a transferência de genes e a formação de micro-consórcios sinérgicos..
-O fenótipo do biofilme pode ser descrito em termos dos genes expressos pelas células associadas. Este fenótipo é alterado em relação à taxa de crescimento e transcrição do gene.
-Os organismos dentro do biofilme podem transcrever genes que não transcrevem suas formas de vida planctônicas ou livres.
-O processo de formação do biofilme é regulado por genes específicos, transcritos durante a adesão celular inicial.
-No espaço confinado da matriz, existem mecanismos de cooperação e competição. A competição gera adaptação constante nas populações biológicas.
-Um sistema digestivo externo coletivo é gerado, que retém as enzimas extracelulares perto das células.
-Este sistema enzimático permite sequestrar, acumular e metabolizar, nutrientes dissolvidos, coloidais e / ou suspensos.
-A matriz funciona como uma área externa comum de reciclagem, um depósito para os componentes das células lisadas, servindo também como um arquivo genético coletivo..
-O biofilme funciona como uma barreira estrutural protetora contra mudanças ambientais, como dessecação, ação de biocidas, antibióticos, respostas imunes do hospedeiro, agentes oxidantes, cátions metálicos, radiação ultravioleta e também é uma defesa contra muitos predadores, como protozoários fagocíticos e insetos..
-A matriz do biofilme constitui um ambiente ecológico único para os microrganismos, permitindo um modo de vida dinâmico para a comunidade biológica. Biofilmes são verdadeiros microecossistemas.
Formação de biofilme
A formação de biofilme é um processo no qual os microrganismos vão de um estado de vida livre, unicelular e nômade para um estado sedentário multicelular, onde o crescimento subsequente produz comunidades estruturadas com diferenciação celular.
O desenvolvimento do biofilme ocorre em resposta a sinais ambientais extracelulares e sinais autogerados.
Pesquisadores que estudaram biofilmes concordam que é possível construir um modelo hipotético generalizado para explicar sua formação..
Este modelo de formação de biofilme consiste em 5 etapas:
- Adesão inicial à superfície.
- Formação de uma monocamada.
- Migração para formar microcolônias multicamadas.
- Produção da matriz extracelular polimérica.
- Maturação do biofilme tridimensional.

Adesão inicial à superfície
A formação do biofilme começa com a adesão inicial dos microrganismos à superfície sólida, onde são imobilizados. Foi descoberto que os microrganismos possuem sensores de superfície e que as proteínas de superfície estão envolvidas na formação da matriz.
Em organismos não móveis, quando as condições ambientais são favoráveis, a produção de adesinas em sua superfície externa aumenta. Dessa forma, aumenta sua capacidade de adesão célula-célula e de superfície celular..
No caso das espécies móveis, os microrganismos individuais estão localizados em uma superfície e este é o ponto de partida para uma mudança radical em seu modo de vida de nômades móveis livres para sedentários, quase sésseis..
A capacidade de movimentação é perdida porque na formação da matriz participam diferentes estruturas como flagelos, cílios, pelos e fímbrias, além de substâncias adesivas..
Então, em ambos os casos (microrganismos móveis e não móveis), pequenos agregados ou microcolônias são formados e um contato célula-célula mais intenso é gerado; mudanças fenotípicas adaptativas ao novo ambiente ocorrem em células agrupadas.
Formação de uma monocamada e microcolônias em multicamadas
Inicia-se a produção de substâncias poliméricas extracelulares, ocorre a formação inicial em monocamada e posterior desenvolvimento em multicamada..
Produção da matriz extracelular polimérica e maturação do biofilme tridimensional
Por fim, o biofilme atinge seu estágio de maturidade, com arquitetura tridimensional e presença de canais por onde circulam água, nutrientes, produtos químicos de comunicação e ácidos nucléicos..
A matriz do biofilme retém as células e as mantém unidas, promovendo um alto grau de interação com a comunicação intercelular e a formação de consórcios sinérgicos. As células do biofilme não estão completamente imobilizadas, elas podem se mover dentro dele e também se desprender.
Tipos de biofilmes
Número de espécies
De acordo com o número de espécies participantes do biofilme, este último pode ser classificado em:
- Biofilmes de uma espécie. Por exemplo, biofilmes feitos de Streptococcus mutans ou Vellionella parvula.
- Biofilmes de duas espécies. Por exemplo, a associação de Streptococcus mutans Y Vellionella parvula em biofilmes.
- Biofilmes polimicrobianos, compostos de muitas espécies. Por exemplo, placa dentária.
Ambiente de treinamento
Também dependendo do ambiente onde são formados, os biofilmes podem ser:
- Natural
- Industrial
- Doméstico
- Hospitaleiro

Tipo de interface onde são gerados
Por outro lado, dependendo do tipo de interface onde se formam, é possível classificá-los em:
- Biofilmes de interface sólido-líquido, como os formados em aquedutos e tanques, tubulações e caixas d'água em geral.
- Biofilmes de interface de gás sólido (SAB por sua sigla em inglês Sub Aereal Biofilms); que são comunidades microbianas que se desenvolvem em superfícies minerais sólidas, diretamente expostas à atmosfera e à radiação solar. Eles são encontrados em edifícios, rochas nuas do deserto, montanhas, entre outros.
Exemplos de biofilmes
-Placa dentária
A placa dentária tem sido estudada como um exemplo interessante de uma comunidade complexa que vive em biofilmes. Os biofilmes das placas dentais são duros e não elásticos, devido à presença de sais inorgânicos, que conferem rigidez à matriz polimérica..
Os microrganismos da placa dentária são muito variados e existem entre 200 a 300 espécies associadas no biofilme..
Entre esses microrganismos estão:
- O genero Estreptococo; composta por bactérias acidúricas que desmineralizam o esmalte e a dentina e iniciam a cárie dentária. Por exemplo, a espécie: mutans, S. sobrinus, S. sanguis, S. salivalis, S. mitis, S. oralis Y S. milleri.
- O genero Lactobacillus, constituído por bactérias acidófilas que desnaturam as proteínas da dentina. Por exemplo, a espécie: casei, L. fermentum, L. acidophillus.
- O genero Actinomyces, que são microrganismos acidúricos e proteolíticos. Entre estas, as espécies: viscosus, A. odontoliticus Y A. naeslundii.
- E outros gêneros, O que: Candida albicans, Bacteroides forsythus, Porphyromonas gingivalis Y Actinobacillus actinomycetecomitans.
-Biofilmes em esgoto
Outro exemplo interessante são os efluentes domésticos, onde vivem em biofilmes presos a tubulações, microrganismos nitrificantes oxidantes de amônio, nitrito e bactérias nitrificantes autotróficas..
Dentre as bactérias oxidantes de amônio desses biofilmes, as espécies numericamente dominantes são as do gênero. Nitrosomonas, distribuído por toda a matriz de biofilme.
A maioria dos componentes dentro do grupo de oxidantes de nitrito são aqueles do gênero Nitrospira, que estão localizados apenas na parte interna do biofilme.
-Biofilmes subaeriais
Os biofilmes subaerie são caracterizados por um crescimento irregular em superfícies minerais sólidas, como rochas e edifícios urbanos. Esses biofilmes apresentam associações dominantes de fungos, algas, cianobactérias, bactérias heterotróficas, protozoários, bem como animais microscópicos..
Em particular, os biofilmes SAB possuem microrganismos quimiolitotróficos, capazes de usar produtos químicos minerais inorgânicos como fontes de energia..
Microrganismos quimiolitotróficos têm a capacidade de oxidar compostos inorgânicos, como Hdois, NH3, NÃOdois, S, HS, Fedois+ e aproveitar a energia do potencial elétrico produto das oxidações em seus metabolismos.
Entre as espécies microbianas presentes em biofilmes subaeriais estão:
- Bactérias do gênero Geodermatophilus; cianobactérias do gênero Chrococcoccidiopsis, espécies cocóides e filamentosas, como Calothrix, Gloeocapsa, Nostoc, Stigonema, Phormidium,
- Algas verdes dos gêneros Chlorella, Desmococcus, Phycopeltis, Printzina, Trebouxia, Trentepohlia e Stichococcus.
- Bactérias heterotróficas (dominantes em biofilmes subaeriais): Arthrobacter sp., Bacillus sp., Micrococcus sp., Paenibacillus sp., Pseudomonas sp. e rodococo sp.
- Bactérias quimioorganotróficas e fungos, como Actynomycetales (estreptomicetos e Geodermatophilaceae), Proteobacteria, Actinobacteria, Acidobacteria e bacteroides-cytophaga-Flavobacterium.
-Biofilmes de agentes causadores de doenças humanas
Muitas das bactérias conhecidas como agentes causadores de doenças humanas vivem em biofilmes. Entre eles estão: Vibrio cholerae, Vibrio parahaemolyticus, Vibrio fischeri, Vellionella parvula, Streptococcus mutans Y Legionella pneumophyla.
-Praga bubÔnica
É interessante a transmissão da peste bubônica pela picada de pulga, uma adaptação relativamente recente do agente bacteriano causador da doença., Yersinia pestis.
Esta bactéria cresce como um biofilme ligado ao trato digestivo superior do vetor (a pulga). Durante uma picada, a pulga regurgita o biofilme contendo Yersinia pestis na derme e, assim, começa a infecção.
-Cateteres venosos hospitalares
Organismos isolados de biofilme em cateteres venosos centrais explantados incluem uma variedade surpreendente de bactérias Gram-positivas e Gram-negativas, bem como outros microorganismos..
Vários estudos científicos relatam como bactérias Gram-positivas de biofilmes em cateteres venosos: Corynebacterium spp., Enterococcus sp., Enterococcus faecalis, Enterococcus faecium, Staphylococcus spp., Estafilococo aureus, Staphylococcus epidermidis, Estreptococo spp. Y Streptococcus pneumoniae.
Entre as bactérias Gram-negativas isoladas desses biofilmes, são relatadas as seguintes: Acinetobacter spp., Acinetobacter calcoaceticus, Acinetobacter anitratus, Enterobacter cloacae, Enterobacter aerogens, Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Pseudomonas aeruginosa, Pseudomonas putida, Proteus spp., Providencia spp. Y Serratia marcescens.
Outros organismos encontrados nesses biofilmes são: Candida spp., Candida albicans, Candida tropicalis Y Mycobacterium chelonei.
-Na indústria
No que se refere ao funcionamento da indústria, os biofilmes geram obstruções em tubulações, danos a equipamentos, interferências em processos como transferência de calor na cobertura de superfícies de trocadores ou corrosão de peças metálicas..
Indústria alimentícia
A formação de filme na indústria de alimentos pode gerar problemas operacionais e de saúde pública significativos.
Patógenos associados em biofilmes podem contaminar produtos alimentícios com bactérias patogênicas e causar sérios problemas de saúde pública para os consumidores.
Entre os biofilmes de patógenos associados à indústria de alimentos estão:
Listeria monocytogenes
Este agente patogênico utiliza na fase inicial de formação de biofilme, flagelos e proteínas de membrana. Forma biofilmes nas superfícies de aço das máquinas de fatiar.
Na indústria de laticínios, biofilmes de Listeria monocytogenes em leite líquido e produtos derivados do leite. Resíduos lácteos em tubulações, tanques, recipientes e outros dispositivos favorecem o desenvolvimento de biofilmes desse patógeno que os utiliza como nutrientes disponíveis..
Pseudomonas spp.
Biofilmes dessas bactérias podem ser encontrados em instalações da indústria de alimentos, como pisos, ralos e nas superfícies de alimentos como carnes, vegetais e frutas, bem como derivados de leite com baixo teor de ácido.
Pseudomonas aeruginosa secreta várias substâncias extracelulares que são utilizadas na formação da matriz polimérica do biofilme, aderindo a um grande número de materiais inorgânicos como o aço inoxidável.
Pseudomonas pode coexistir dentro do biofilme em associação com outras bactérias patogênicas, como Salmonella Y Listeria.
Salmonella spp.
As espécies de Salmonella são o primeiro agente causal de zoonoses de etiologia bacteriana e surtos de toxoinfecção alimentar.
Estudos científicos têm mostrado que Salmonella pode aderir como biofilmes a superfícies de concreto, aço e plástico em instalações de processamento de alimentos.
As espécies de Salmonella eles têm estruturas de superfície com propriedades aderentes. Além disso, produz celulose como substância extracelular, principal componente da matriz polimérica..
Escherichia coli
Ele usa flagelos e proteínas de membrana na etapa inicial da formação do biofilme. Ele também produz celulose extracelular para gerar a rede tridimensional da matriz no biofilme..
Resistência de biofilmes a desinfetantes, germicidas e antibióticos
Os biofilmes oferecem proteção aos microrganismos que os compõem, à ação de desinfetantes, germicidas e antibióticos. Os mecanismos que permitem esse recurso são os seguintes:
- Retardo na penetração do agente antimicrobiano através da matriz tridimensional do biofilme, devido à difusão muito lenta e dificuldade em atingir a concentração efetiva.
- Taxa de crescimento alterada e baixo metabolismo de microrganismos no biofilme.
- Alterações nas respostas fisiológicas dos microrganismos durante o crescimento do biofilme, com alteração da expressão do gene de resistência.
Referências
- Biofilmes bacterianos. (2008). Tópicos Atuais em Microbiologia e Imunologia. Editor Tony Romeo. Vol. 322. Berlin, Hannover: Springer Verlag. pp301.
- Donlan, R.M. e Costerton, J.W. (2002). Biofilmes: mecanismos de sobrevivência de microrganismos clinicamente relevantes. Avaliações de Microbiologia Clínica.15 (2): 167-193. doi: 10.1128 / CMR.15.2.167-193.2002
- Fleming, H.C. e Wingender, F. (2010). A matriz de biofilme. Nature Reviews Microbiology. 8: 623-633.
- Gorbushina, A. (2007). Vida nas rochas. Microbiologia Ambiental. 9 (7): 1-24. doi: 10.1111 / j.1462-2920.2007.01301.x
- O'Toole, G., Kaplan, H.B. e Kolter, R. (2000). Formação de biofilme como desenvolvimento microbiano. Revisão Anual de Microbiologia. 54: 49-79. doi: 1146 / annurev.microbiol.54.1.49
- Hall-Sstandley, L., Costerton, J.W. e Sstandley, P. (2004). Biofilmes bacterianos: do ambiente natural às doenças infecciosas. Nature Reviews Microbiology. 2: 95-108.
- Whitchurch, C.B., Tolker-Nielsen, T., Ragas, P. e Mattick, J. (2002). DNA extracelular necessário para a formação de biofilme bacteriano. 259 (5559): 1487-1499. doi: 10.1126 / science.295.5559.1487



Ainda sem comentários