
Características do ácido hipobromoso, estrutura, usos

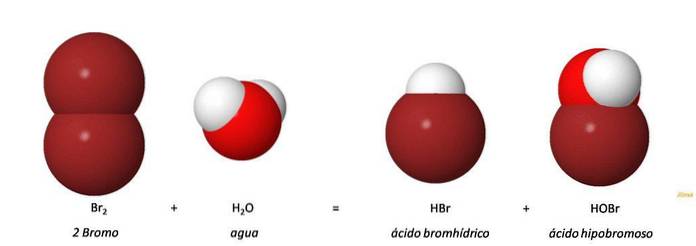
O ácido hipobromoso (HOBr, HBrO) é um ácido inorgânico produzido pela oxidação do ânion brometo (Br-). A adição de bromo à água dá ácido bromídrico (HBr) e ácido hipobromoso (HOBr) por meio de uma reação de desproporção. Br2 + H2O = HOBr + HBr
O ácido hipobromoso é um ácido muito fraco, um tanto instável, existindo como uma solução diluída à temperatura ambiente. É produzida em organismos vertebrados de sangue quente (incluindo humanos), pela ação da enzima eosinófila peroxidase.
A descoberta de que o ácido hipobromoso pode regular a atividade do colágeno IV atraiu muita atenção..
Índice do artigo
- 1 Estrutura
- 1.1 2D
- 1.2 3D
- 2 Propriedades físicas e químicas
- 3 usos
- 4 interações biomoleculares
- 5 referências
Estrutura
2D
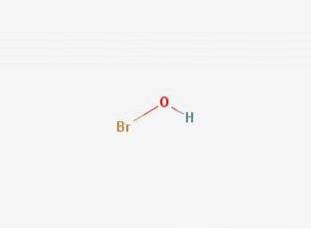
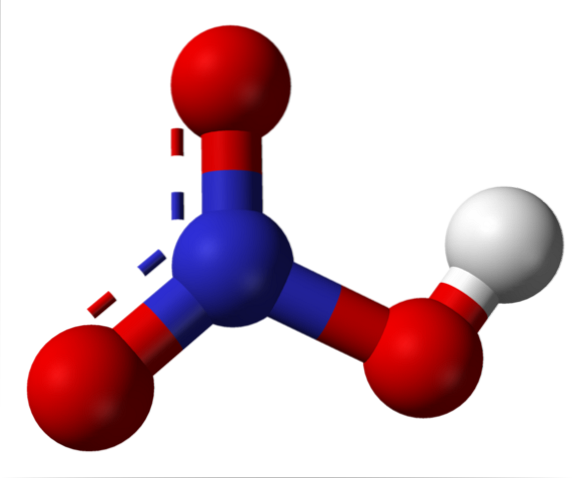
3D

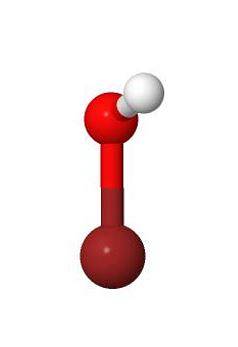
Propriedades físicas e químicas
- Sólidos amarelos de aparência: sólidos amarelos.
- Aparência: sólidos amarelos.
- Peso molecular: 96,911 g / mol.
- Ponto de ebulição: 20-25 ° C.
- Densidade: 2,470 g / cm3.
- Acidez (pKa): 8,65.
- As propriedades químicas e físicas do ácido hipobromoso são semelhantes às de outros hipohalitos..
- Ele vem como uma solução diluída em temperatura ambiente.
- Os sólidos de hipobromito são de cor amarela e têm um odor aromático peculiar.
- É um forte bactericida e desinfetante de água.
- Tem um pKa de 8,65 e se dissocia parcialmente em água a pH 7.
Formulários
- O ácido hipobromoso (HOBr) é utilizado como agente clareador, oxidante, desodorante e desinfetante, devido à sua capacidade de matar as células de muitos patógenos.
- É utilizado pela indústria têxtil como agente de branqueamento e secagem.
- Também usado em banheiras de hidromassagem e spas como agente germicida.
Interações biomoleculares
O bromo é onipresente em animais como brometo iônico (Br-), mas até recentemente sua função essencial era desconhecida..
Uma pesquisa recente mostrou que o bromo é essencial para a arquitetura da membrana basal e desenvolvimento de tecidos.
A enzima peroxidina usa HOBr para reticular a sulfilimina, que é reticulada nas estruturas de colágeno IV da membrana basal..
O ácido hipobromoso é produzido em organismos vertebrados de sangue quente pela ação da enzima eosinófila peroxidase (EPO).
A EPO gera HOBr a partir de H2O2 e Br- na presença de uma concentração plasmática de Cl-.
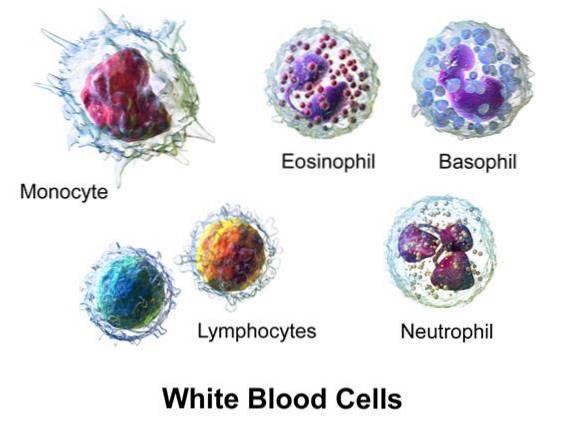
A mieloperoxidase (MPO), a partir de monócitos e neutrófilos, gera ácido hipocloroso (HOCl) a partir de H2O2 e Cl-.
EPO e MPO desempenham um papel importante nos mecanismos de defesa do hospedeiro contra patógenos, usando HOBr e HOCl, respectivamente.
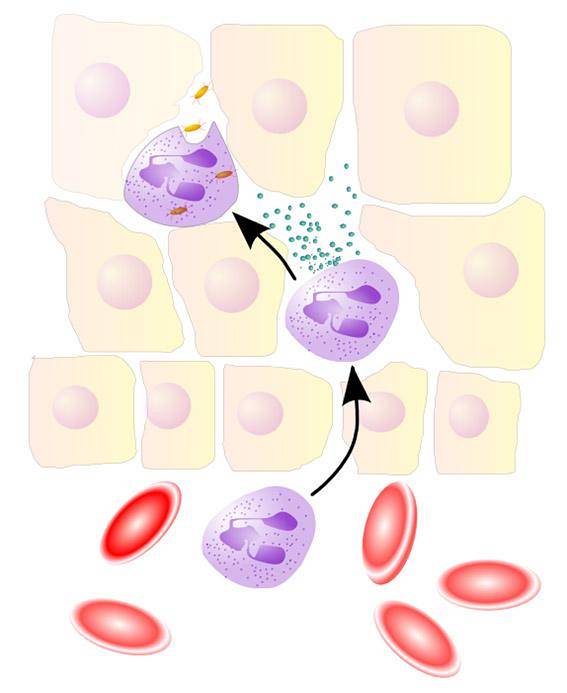
O sistema MPO / H2O2 / Cl- na presença de Br- também gera HOBr ao reagir o HOCl formado com Br-. Mais do que um oxidante poderoso, HOBr é um eletrófilo poderoso.
A concentração plasmática de Br- é mais de 1000 vezes menor do que a do ânion cloreto (Cl-). Consequentemente, a produção endógena de HOBr também é menor em comparação com HOCl.
No entanto, o HOBr é significativamente mais reativo do que o HOCl quando a oxidabilidade dos compostos estudados não é relevante, portanto a reatividade do HOBr poderia estar mais associada à sua força eletrofílica do que ao seu poder oxidante (Ximenes, Morgon & de Souza, 2015).
Embora seu potencial redox seja inferior ao do HOCl, o HOBr reage com os aminoácidos mais rápido do que o HOCl.
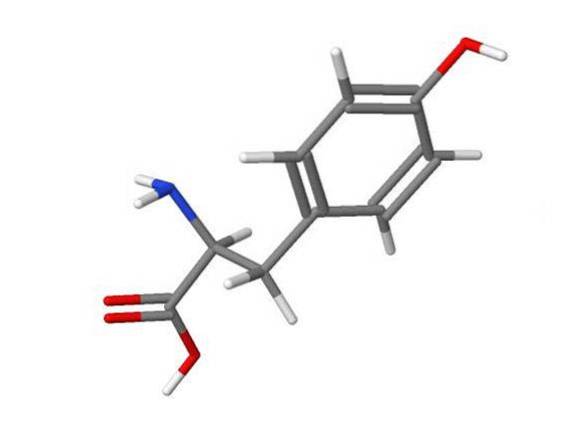
A halogenação do anel de tirosina pelo HOBr é 5000 vezes mais rápida que a do HOCl.
HOBr também reage com nucleobases de nucleosídeos e DNA.
2'-desoxicitidina, adenina e guanina, geram 5-bromo-2'-desoxicitidina, 8-bromoadenina e 8-bromoguanina em EPO / H2O2 / Br- e sistemas MPO / H2O2 / Cl- / Br- (Suzuki, Kitabatake e Koide , 2016).
McCall, et al. (2014) demonstraram que o Br é um cofator necessário para a formação de ligações cruzadas de sulfilimina catalisadas pela enzima peroxidasina, uma modificação pós-tradução essencial para a arquitetura do colágeno IV das membranas basais e o desenvolvimento dos tecidos..
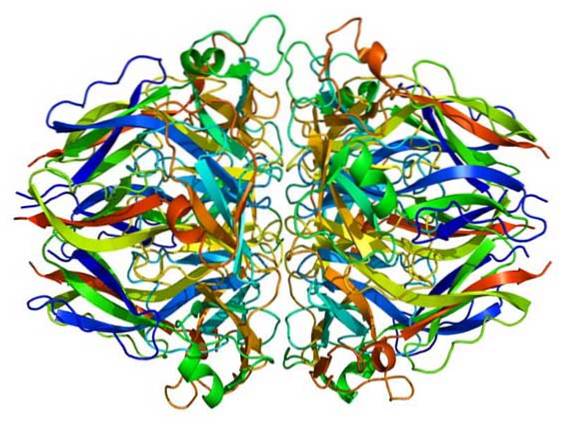
As membranas basais são matrizes extracelulares especializadas que são mediadores-chave da transdução de sinal e suporte mecânico das células epiteliais..
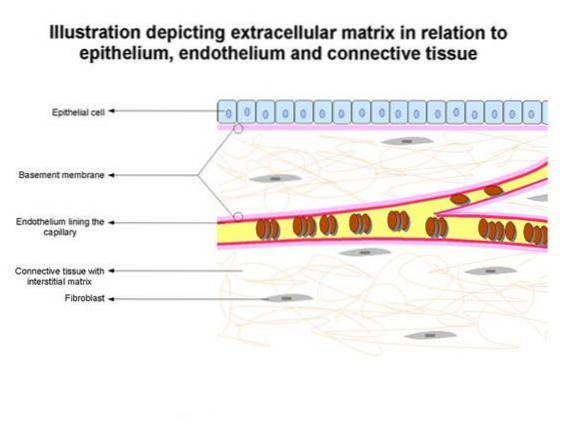
As membranas basais definem a arquitetura do tecido epitelial e facilitam o reparo do tecido após a lesão, entre outras funções..
Embutido na membrana basal está um andaime de colágeno IV reticulado com sulfilimina, que fornece a funcionalidade de matriz em tecidos multicelulares de todos os animais..
Os andaimes de colágeno IV fornecem resistência mecânica, servem como ligantes para integrinas e outros receptores de superfície celular e interagem com fatores de crescimento para estabelecer gradientes de sinalização..
Sulfilimina (sulfimida) é um composto químico que contém uma ligação dupla de enxofre para nitrogênio. As ligações de sulfilimina estabilizam os filamentos de colágeno IV encontrados na matriz extracelular.
Estas ligações ligam covalentemente os resíduos de metionina 93 (Met93) e hidroxilisina 211 (Hyl211) de cadeias polipeptídicas adjacentes para formar um trímero de colágeno maior..
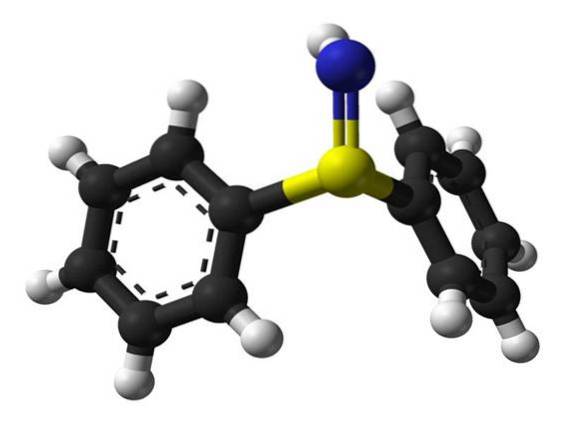
A peroxidina forma ácido hipobromoso (HOBr) e ácido hipocloroso (HOCl) a partir do brometo e do cloreto, respectivamente, que podem mediar a formação de reticulações de sulfilimina..
O brometo, convertido em ácido hipobromoso, forma um intermediário do íon bromossulfônio (S-Br) que participa da formação de ligações cruzadas..
McCall, et al. (2014) demonstraram que a deficiência de Br na dieta é letal na mosca Drosophila, enquanto a reposição de Br restaura sua viabilidade..
Eles também estabeleceram que o bromo é um oligoelemento essencial para todos os animais devido ao seu papel na formação de ligações sulfilimina e colágeno IV, que é de vital importância para a formação das membranas basais e o desenvolvimento dos tecidos..
Referências
- ChemIDplus, (2017). Estrutura 3D de 13517-11-8 - ácido hipobromoso [imagem] Recuperado de nih.gov.
- ChemIDplus, (2017). Estrutura 3D de 60-18-4 - Tirosina [USAN: INN] [imagem] Obtido em nih.gov.
- ChemIDplus, (2017). Estrutura 3D de 7726-95-6 - Bromo [imagem] Recuperado de nih.gov.
- ChemIDplus, (2017). Estrutura 3D de 7732-18-5 - Água [imagem] Recuperado de nih.gov.
- Emw, (2009). Proteína COL4A1 PDB 1li1 [imagem] Recuperada de wikipedia.org.
- Mills, B. (2009). Diphenylsulfimide-from-xtal-2002-3D-balls [imagem] Recuperado de wikipedia.org.
- PubChem, (2016). Ácido hipobromoso [imagem] Obtido em nih.gov.
- Steane, R. (2014). A molécula de DNA - giratória em 3 dimensões [imagem] Recovered from biotopics.co.uk
- Thormann, U. (2005). NeutrophilerAktion [imagem] Recuperado de wikipedia.org.
Ainda sem comentários