
Estrutura, propriedades, riscos e usos do álcool butílico terciário
O álcool butílico terciário é um composto orgânico cuja fórmula é (CH3)3COH ou t-BuOH. É o álcool terciário mais simples de todos. Dependendo da temperatura ambiente, ele aparece como um sólido ou líquido incolor. A imagem abaixo mostra, por exemplo, seus cristais incolores.
Este álcool não é substrato para a enzima desidrogenase alcoólica, nem para a atividade peroxidase da catalase, portanto é classificado como um álcool não metabolizável. Devido às suas propriedades bioquímicas, acredita-se que possa ser útil na detecção de radicais hidroxila in vivo em células intactas..

É um dos quatro isômeros do álcool isobutílico, sendo o isômero o menos suscetível à oxidação e o menos reativo. Na natureza, é encontrada no grão de bico e na mandioca ou mandioca, raiz que é fermentada para a produção de bebidas alcoólicas..
O álcool butílico terciário é muito solúvel em água e solventes orgânicos. Seu principal uso é como solvente, cumprindo essa função na produção de plásticos, perfumes, removedores de tinta, etc..
Como muitos compostos orgânicos, é um pouco tóxico, mas em altas doses tem um efeito narcótico, caracterizado por dores de cabeça, vertigens, vertigens, vertigens e vertigens..
Índice do artigo
- 1 Estrutura do álcool terc-butílico
- 2 propriedades
- 2.1 Nomes químicos
- 2.2 Fórmula molecular
- 2.3 Peso molecular
- 2.4 Descrição física
- 2,5 Odor
- 2.6 Ponto de ebulição
- 2.7 Ponto de fusão
- 2.8 ponto de fulgor
- 2.9 Solubilidade em água
- 2.10 Solubilidade em solventes orgânicos
- 2.11 Densidade
- 2,12 Densidade de vapor
- 2.13 Pressão de vapor
- 2.14 Coeficiente de partição octanol / água
- 2.15 Termostabilidade
- 2.16 Temperatura de autoignição
- 2.17 Decomposição
- 2,18 Calor de vaporização
- 2,19 capacidade calórica
- 2.20 Entalpia de formação
- 2.21 Temperatura de armazenamento
- 2.22 Estabilidade
- 2.23 Potencial de ionização
- 2.24 Limite de odor
- 2,25 Índice de refração
- 2.26 Constante de dissociação
- 2.27 Concentração máxima de vapor
- 2.28 Reações
- 3 riscos
- 4 usos
- 5 referências
Estrutura do álcool terc-butílico
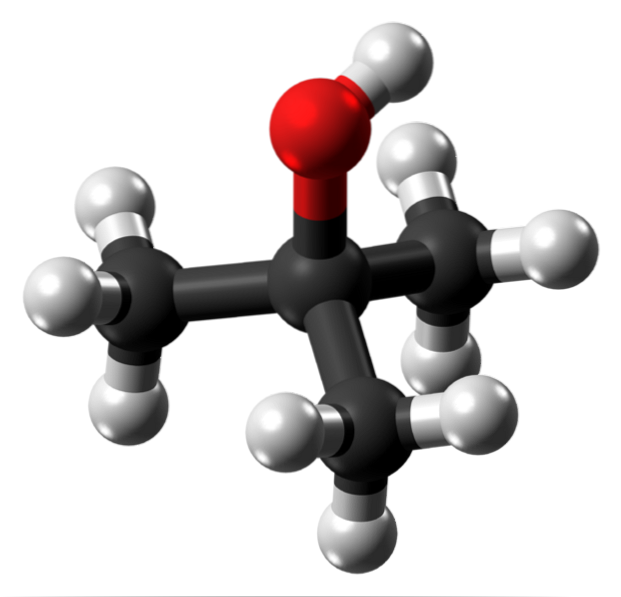
A imagem superior mostra a estrutura molecular do álcool terc-butílico com um modelo de esferas e barras. A molécula inteira tem uma geometria tetraédrica global, com o terceiro carbono localizado em seu centro, e os grupos CH3 e OH em seus vértices.
Observando essa estrutura, entende-se por que esse álcool é terciário: o carbono do centro está ligado a três outros carbonos. Continuando com o tetraedro, sua parte inferior pode ser considerada apolar, enquanto seu vértice superior, polar.
Neste vértice está o grupo OH, que cria um momento dipolar permanente e também permite que as moléculas de t-BuOH interajam por meio de ligações de hidrogênio; da mesma forma que faz com as moléculas de água e outras substâncias polares.
Nos cristais de t-BuOH, essas ligações de hidrogênio são um fator chave para que as moléculas permaneçam juntas; embora não haja muitas informações sobre qual é a estrutura cristalina deste álcool.
Como o grupo OH está tão próximo e rodeado pelos grupos apolares CH3, as moléculas de água conseguem hidratar quase todo o álcool ao mesmo tempo que interagem com o OH. Isso explicaria sua grande solubilidade em água..
Propriedades
Nomes químicos
-Álcool butílico terciário
-terc-butanol
-2-metil-2-propanol
-2-metilpropan-2-ol.
Fórmula molecular
C4H10O ou (CH3)3COH.
Peso molecular
74,123 g / mol.
Descrição física
Sólido incolor ou líquido incolor, dependendo da temperatura ambiente, pois o ponto de fusão é 77,9ºF (25,4ºC). Acima de 77,9ºF é um líquido.
Odor
Semelhante a cânfora.
Ponto de ebulição
82,4 ºC.
Ponto de fusão
77,9 ºF (25,4 ºC).
ponto de ignição
52 ° F (11 ° C). Taça fechada.
Solubilidade em água
Muito solúvel. Na verdade, independentemente das proporções, esse álcool é sempre miscível com água..
Solubilidade em solventes orgânicos
Miscível com etanol, éter etílico e solúvel em clorofórmio.
Densidade
0,78 g / cm3.
Densidade do vapor
2,55 (em relação ao ar = 1).
Pressão de vapor
4,1 kPa a 20 ºC.
Coeficiente de partição octanol / água
Log P = 0,35.
Termoestabilidade
Instável no calor
Temperatura de autoignição
896 ºF (470 ºC).
Decomposição
Quando aquecido, pode liberar vapores de monóxido de carbono e isobutileno.
Calor da vaporização
39,07 kJ / mol.
Capacidade calórica
215,37 JK-1toupeira-1.
Entalpia de formação
-360,04 a -358,36 kJmol-1.
Temperatura de armazenamento
2-8 ºC.
Estabilidade
É estável, mas incompatível com agentes oxidantes fortes, cobre, ligas de cobre, metais alcalinos e alumínio.
Potencial de ionização
9,70 eV.
Limiar de odor
219 mg / m3 (baixo odor).
Índice de refração
1.382 a 25 ºC.
Constante de dissociação
pKa = 19,20.
Concentração máxima de vapor
5,53% a 25 ºC.
Reações
-É desprotonado por uma base forte para dar origem a um ânion alcóxido; especificamente, um terbutóxido, (CH3)3CO-.
-O álcool butílico terciário reage com o cloreto de hidrogênio para formar o cloreto butílico terciário..
(CH3)3COH + HCl => (CH3)3CCl + HdoisOU
Álcoois terciários têm maior reatividade com haletos de hidrogênio do que álcoois secundários e primários.
Riscos
O álcool tert-butílico em contato com a pele causa lesões menores, como eritema não grave e hiperemia. Além disso, não passa pela pele. Pelo contrário, nos olhos, produz irritação severa.
Quando inalado, irrita o nariz, a garganta e os brônquios. Em caso de alta exposição, podem ocorrer efeitos narcóticos, um estado de sonolência, bem como tontura, tontura e dor de cabeça.
Este álcool é um agente teratogênico experimental, por isso tem sido observado em animais que pode influenciar o aparecimento de doenças congênitas.
Quanto ao seu armazenamento, seu líquido e vapores são inflamáveis, podendo em determinadas circunstâncias gerar incêndios e explosões..
OSHA estabeleceu um limite de concentração de 100 ppm (300 mg / m3) por um turno de 8 horas.
Formulários
-O álcool terc-butílico é utilizado para a incorporação do grupo terc-butil em compostos orgânicos, para a preparação de resinas solúveis em óleo, e o trinitro-terc-butiltolueno, um almíscar artificial. Além disso, constitui um material de partida para a preparação de peróxidos.
-Foi aprovado pelo FDA como agente antiespumante para uso em materiais e componentes plásticos que entram em contato com alimentos. Tem sido utilizado na produção de essências de frutas, plásticos e lacas..
-É um intermediário para a produção de cloreto de terc-butila e tributilfenol. Atua como agente desnaturante para etanol.
-É utilizado na fabricação de agentes de flotação, como solvente orgânico para remover tintas e dissolver essências utilizadas em perfumes..
-É usado como um intensificador de octanas na gasolina; combustível e aditivo de combustível; solvente para ser usado na limpeza e como desengraxante.
-O álcool terc-butílico é um agente intermediário na produção de éter terc-butilmetílico (MTBE) e éter tributiletílico (ETBE), reagindo respectivamente com metanol e etanol.
-Também atua da mesma forma na produção do hidroperóxido de tributil (TBHP) por reação com o peróxido de hidrogênio..
-É usado como reagente no processo conhecido como rearranjo de Curtius..
Referências
- Graham Solomons T.W., Craig B. Fryhle. (2011). Química orgânica. Aminas. (10º edição.). Wiley plus.
- Wikipedia. (2019). Álcool tert-butílico. Recuperado de: en.wikipedia.org
- CommonOrganicChemistry. (s.f.). t-Butanol. Recuperado de: commonorganicchemistry.com
- Centro Nacional de Informações sobre Biotecnologia. (2019). Tert butanol. Banco de dados PubChem. Recuperado de: pubchem.ncbi.nlm.nih.gov
- Carey F. A. (2008). Quimica Organica. (Sexta edição). Mc Graw Hill.



Ainda sem comentários